El futuro para detener hemorragias se encuentra en la jeringuilla XStat

La jeringuilla XSTAT es un dispositivo hemostático impar diseñado para el tratamiento de heridas de tiros y astillas en el campo de batalla. Las hemorragias son la causa de hasta un 40% de las muertes de civiles por traumatismos. Y hasta un 56% de esos casos ocurren antes de llegar al hospital.

Es por eso que la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha autorizado el uso médico de una jeringa que permite tapar heridas de bala en sólo unos pocos segundos.
El invento recibe el nombre de XSTAT 30 y es una jeringuilla rellena de pequeñas esponjas esterilizadas.
Una vez que la jeringuilla se introduce en la herida, las esponjas se hinchan y la taponan para detener la hemorragia.
Así evitar así que la víctima muera desangrada y pueda llegar a quirófano.
La jeringuilla XSTAT 30, un dispositivo que sella heridas de bala en segundos.
Cada inyección puede absorber hasta medio litro de sangre y el proceso dura 15 segundos.
Hasta el momento esta técnica se usaba sólo en el ejército.
El sistema sólo estaba autorizado para uso militar, pero de ahora en adelante también se va a poder usar en ambulancias y hospitales.
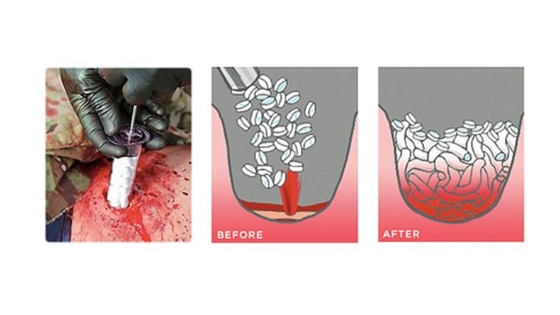
En la herida, el XStat® se expande y se adapta, en contacto con la sangre.
Llenando la cavidad en hasta 20 segundos.
Lo que crea una barrera para el flujo de sangre y proporciona presión hemostática.
La FDA ha pedido el uso responsable de la jeringuilla XSTAT 30 en situaciones en que no haya otra alternativa para frenar el sangrado.
Han informado que este dispositivo no puede ser aplicado en determinadas partes del cuerpo .Como el pecho, el abdomen, la pelvis o por encima de la clavícula.
Manifestando a su vez, que dicho apósito sólo puede ser usado durante un máximo de cuatro horas.
Tiempo que permitiría que el paciente reciba atención quirúrgica.
XStat® es un dispositivo innovador
Que puede ser empleado rápidamente, permitiendo un control hemorrágico inmediato para estabilizar a un paciente para el transporte.
Afirma Christy Foreman, director de la oficina de evaluación de dispositivos de la FDA.

 Italian
Italian Portuguese
Portuguese Spanish
Spanish German
German







